Nature Communications | 刘聪团队与合作者揭示患者来源TTR病理聚集体结构及其小分子探针识别机制
转甲状腺素蛋白淀粉样变性(transthyretin amyloidosis,ATTR)是一类由TTR蛋白错误折叠并沉积引起的系统性疾病,主要累及周围神经系统和心脏。正常情况下,TTR以稳定四聚体形式存在;病理状态下,四聚体解离为单体并聚集形成淀粉样纤维,是ATTR发生的关键分子基础[1]。根据是否存在TTR基因突变,ATTR可分为遗传型ATTR(variant,ATTRv)和野生型ATTR(wildtype,ATTRwt)。ATTRv由TTR基因突变导致,ATTRwt患者TTR氨基酸序列正常,其蛋白解离和沉积机制尚未完全阐明。
近年来研究显示,ATTRwt隐匿性强,大量患者未能及时诊断。尸检研究发现,25%的85岁以上人群心脏中存在TTR沉积[2];在50岁以上、伴射血分数保留心力衰竭和左室肥厚的患者中,18.8%被诊断为ATTR心脏淀粉样变(ATTR-CM),其中绝大多数为ATTRwt[3]。ATTRwt主要累及心脏,可导致心室壁增厚、进行性心力衰竭和心律失常,因此,提示早期、敏感的检测手段仍是重要临床需求。目前,脂肪组织活检结合刚果红(Congo Red,CR)染色常用于辅助诊断ATTR-CM,该手段相比心肌活检更安全、可行,但脂肪组织中TTR淀粉样纤维的结构特征及其与染料分子的互作机制此前仍不清楚。
2026年4月24日,中国科学院上海有机化学研究所生物与化学交叉研究中心刘聪团队联合上海交通大学Bio-X研究院李丹团队及中南大学湘雅三医院张如旭团队在Nature Communications发表题为“Structures of dye-bound transthyretin amyloid fibrils from abdominal fat biopsies”的研究论文,解析了患者脂肪活检组织来源的TTR淀粉样纤维结构,并揭示了CR和硫磺素S(Thioflavin S,ThS)的结合模式。该研究证明脂肪组织与心肌组织来源的TTR淀粉样纤维具有相似结构,为ATTR临床诊断及小分子示踪剂设计提供了结构基础。

研究者收集了3例ATTR-Ala97Ser患者的腹部脂肪组织活检样本,并通过组织切片染色证实其中存在大量TTR淀粉样纤维。随后,研究者提取并纯化脂肪组织中的纤维成分,利用负染透射电镜观察其形态,并进一步通过冷冻电镜解析其高分辨率结构(图1)。结果显示,脂肪组织来源的TTR淀粉样纤维与既往报道的心脏来源纤维结构高度一致,均呈现典型的cross-β折叠和“closed-gate”构象。该结果不仅为脂肪活检用于ATTR诊断提供了直接结构依据,也表明Ala97Ser突变型TTR纤维与多数已报道的突变型及野生型TTR淀粉样纤维具有相似结构,从而为TTR淀粉样纤维诊断探针和靶向药物的开发提供了重要结构基础。
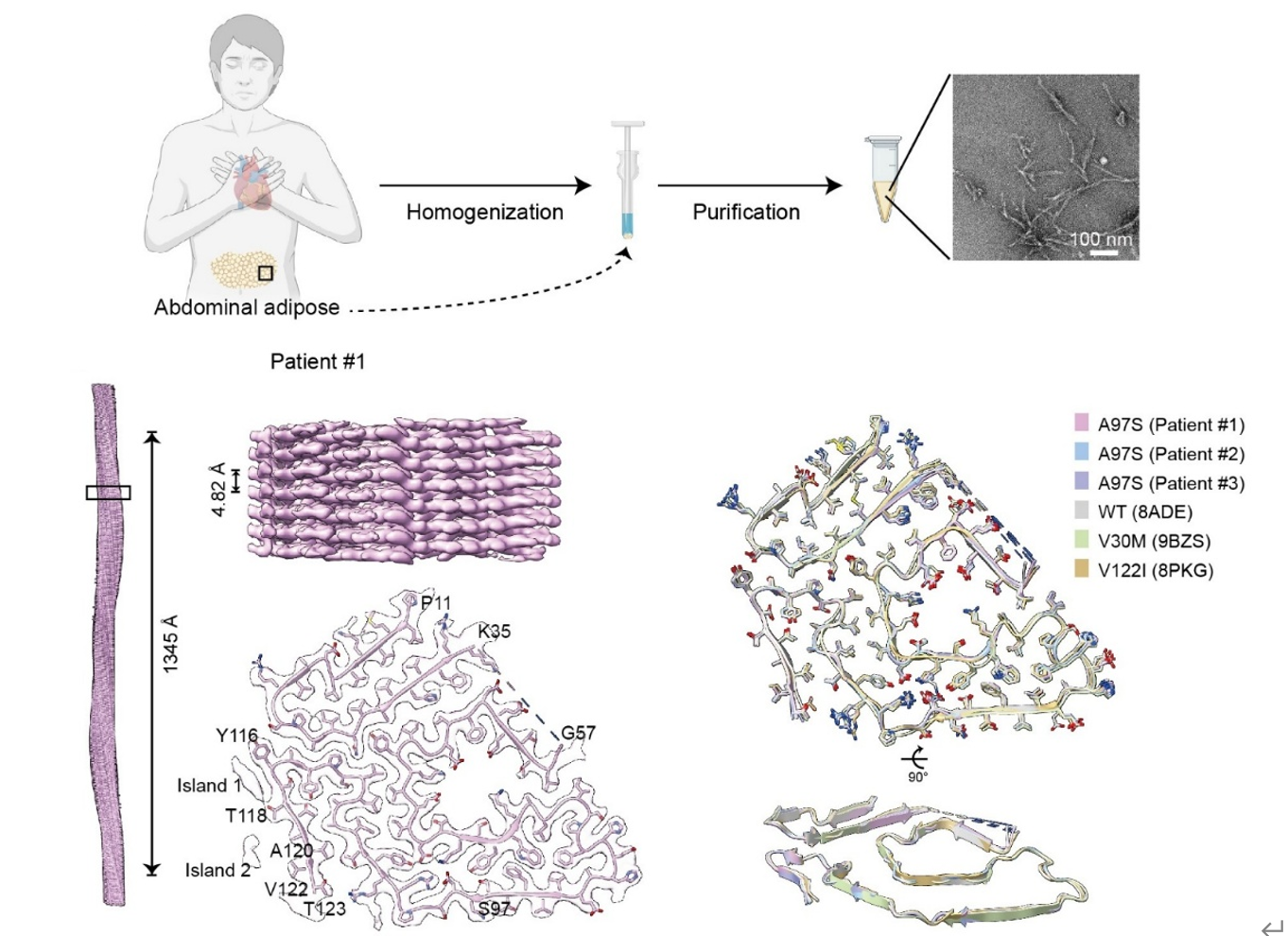
图1. ATTR患者腹壁脂肪组织活检样本中TTR淀粉样纤维的提取与结构解析。Patient #1脂肪组织来源TTR淀粉样纤维的冷冻电镜结构,以及三例患者脂肪组织来源纤维与既往报道的野生型和突变型TTR淀粉样纤维的结构比较。
在获得高分辨率结构后,研究进一步解析了经典染料分子与TTR淀粉样纤维的相互作用机制。结果显示,CR与ThS虽然分子结构不同,但二者在结合策略上具有显著共性:均优先识别纤维表面带正电的区域,尤其是以Arg21为核心的结合口袋,并通过小分子磺酸基团与Arg侧链之间的静电作用实现稳定结合。结构分析表明,CR和ThS均以“vertical”模式结合TTR淀粉样纤维,这也是小分子识别淀粉样纤维的经典结合方式之一[4]。
与此同时,CR与ThS的结合模式也存在明显差异。CR除稳定结合Arg21位点外,还可在Arg104附近形成第二结合位点;而ThS主要局限于Arg21区域,在Arg104处仅表现出较弱或瞬时相互作用。此外,CR在Val94和Val122附近还存在两个由疏水相互作用介导的不稳定结合位点,而ThS在相应区域未观察到明确结合。CR和ThS识别TTR淀粉样纤维的分子机制总结见图2。
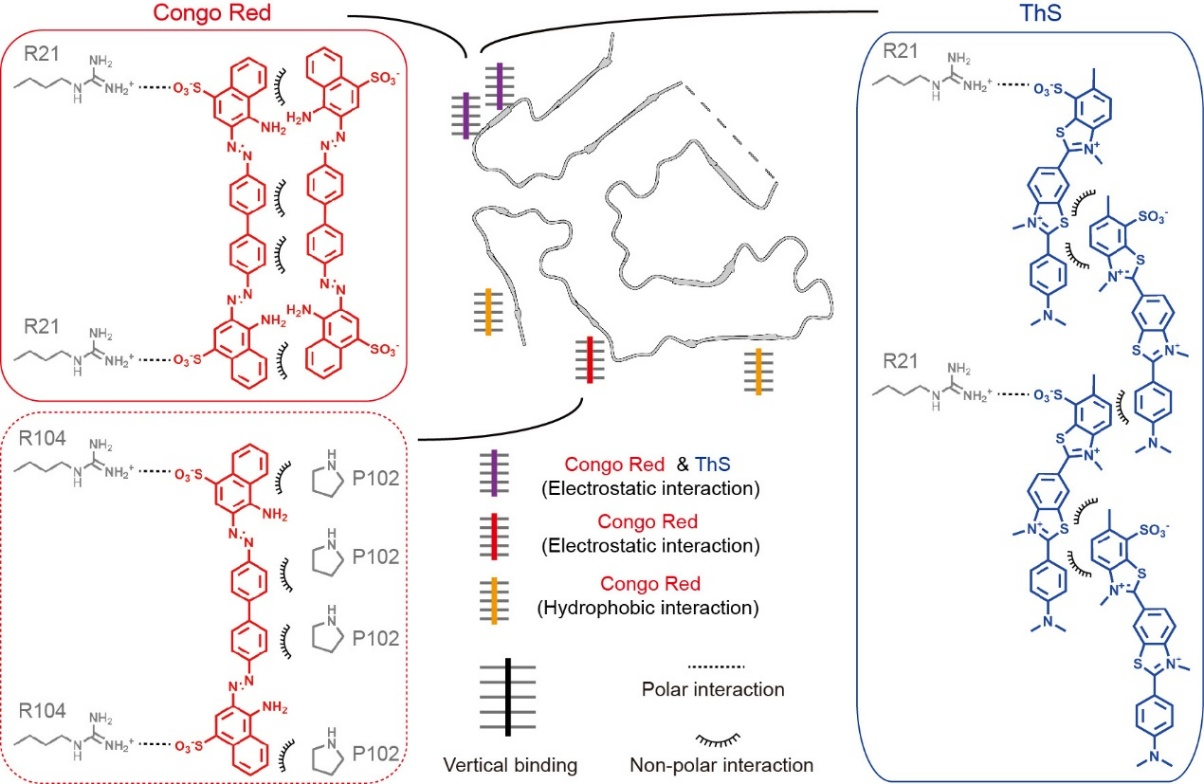
图2. TTR淀粉样纤维与经典染料结合的机制模型。CR和ThS均可通过磺酸基团与Arg21附近的正电口袋发生静电相互作用,并沿纤维轴方向呈垂直排列;CR还可进一步结合Arg104附近位点,并与部分疏水区域发生相互作用。
这项工作首次系统解析了患者脂肪活检组织来源TTR淀粉样纤维的高分辨率结构,证明其与心肌组织来源纤维在整体构象上高度一致,为脂肪组织活检用于ATTR临床诊断提供了直接的结构依据。同时,研究在原子水平揭示了刚果红和硫磺素S等经典小分子探针识别TTR病理性纤维的分子机制,解释了传统染料用于淀粉样纤维检测的结构基础。该发现不仅加深了对TTR淀粉样纤维组织沉积和分子识别规律的理解,也为开发更高灵敏度、更高特异性的ATTR诊断探针、影像示踪剂及靶向干预分子提供了重要参考。
本研究由中国科学院上海有机化学研究所生物与化学交叉研究中心刘聪研究员、上海交通大学Bio-X研究院张江高等研究院李丹教授和中南大学附属湘雅三医院张如旭教授担任共同通讯作者。中国科学院上海有机化学研究所生物与化学交叉研究中心博士后马博远、上海交通大学Bio-X研究院张江高等研究院博士研究生姚语萱和中南大学附属湘雅三医院博士研究生王清萍为共同第一作者。本研究受到中国科学院,国家自然科学基金委,上海市科委及上海尚思自然科学研究院的支持。
参考文献
[1] 转甲状腺素蛋白淀粉样变性诊疗指南2025. 国卫办医政函〔2025〕252号.
[2] Tanskanen M, Peuralinna T, Polvikoski T, et al. Senile systemic amyloidosis affects 25% of the very aged and associates with genetic variation in alpha2‐macroglobulin and tau: a population‐based autopsy study[J]. Annals of medicine, 2008, 40(3): 232-239.
[3] Garcia-Pavia P, Damy T, Piriou N, et al. Prevalence and characteristics of transthyretin amyloid cardiomyopathy in hypertrophic cardiomyopathy[J]. ESC Heart Failure, 2024, 11(6): 4314-4324.
[4] Tao Y, Xia W, Zhao Q, et al. Structural mechanism for specific binding of chemical compounds to amyloid fibrils[J]. Nature Chemical Biology, 2023, 19(10): 1235-1245.
原文链接:https://www.nature.com/articles/s41467-026-72441-5
附件下载:

